|
近日关于PD-1/L1+ADC的好消息不断。
前不久,国家药监局(NMPA)官网公示信息,阿斯利康和第一三共联合开发的注射用德曲妥珠单抗(DS-8201)正式在中国获批上市。

公开资料显示,德曲妥珠单抗是一款靶向HER2的抗体偶联药物(ADC),已在海外获批多种适应症。本次为该药首次在中国获批,针对的适应症为:单药适用于治疗既往接受过一种或一种以上抗HER2药物治疗的不可切除或转移性HER2阳性成人乳腺癌患者。
无独有偶,就在昨日,恒瑞医药自主研发的PD-L1单抗阿得贝利单抗注射液获得NMPA批准上市,本次获批的适应症为联合化疗一线治疗广泛期小细胞肺癌(EC-SCLC),这是恒瑞2023年首个获批上市的创新药,也是首个获批上市的国产PD-L1单抗。另一方面,恒瑞也在积极布局ADC领域,7款药物处于不同研发阶段。在PD-1/PD-L1双抗和ADC两项前沿技术的布局上,恒瑞医药皆跑在了国内前头。
与此同时,科伦博泰与默沙东正合作开发的创新TROP2-ADC联合帕博利珠单抗,用于选定的晚期实体瘤患者的II期临床研究,在中国完成首例患者给药。本研究SKB264-II-06是一项国际多中心临床研究,拟在中国、美国、加拿大、澳大利亚、欧洲国家等多国开展。
此外,还有中国首款CLDN18.2 ADC新药CMG901(由乐普生物负责ADC技术、康诺亚负责抗体)以11.88亿美元总金额授权给阿斯利康。
ADC药物被看做是市场的下一波重磅药品,而作为曾经备受市场热捧的PD-1/L1药物,多家企业也开始通过ADC联合使用希望能够碰撞出新的火花和潜力市场。
在业内看来,ADC是一个技术路线,PD-1是一个靶点,ADC药物在很多不同靶点的探索,PD-1/L1+ADC的联合疗法是否能够呈现“1+1>2”的效果,似乎正在得到跨国药企和本土药企越来越多的关注。
跨国药企强强联手
ADC+PD-1相关研究“狂飙”
作为开启抗体药物时代的重要靶点,PD-1/L1药物在全球掀起的肿瘤免疫治疗市场风潮,如今细分领域的发展局面已经开始进入成熟期。为了进一步延伸肿瘤免疫治疗的产品生命周期,跨国药企已经开始行动,通过联合ADC药物力求保持市场领先,多个PD-1/L1药物和ADC联合治疗相关临床试验已经在进行中。
全球MNC中,默沙东最有动力布局“PD-1/L1+ADC”。伴随去年400亿美元收购Seagen的传言开始消散,默沙东快速转向与科伦展开多项合作,引进9个ADC项目,合作总金额116亿美元,引发市场关注。
业内专家分析认为,默沙东把下一代重磅药物的希望聚焦在ADC领域,主要的目的还是为了进一步巩固旗下Keytruda未来“新药王”地位。
这一观点很快得到了证实。今年2月7日,科伦药业一份最新的交流纪要,管理层提到:“默沙东看重科伦博泰ADC,在很大程度上也是看重与K药联合的潜力,从而进一步可延长K药的生命周期,继续保持K药的地位。”


此外,阿斯利康也对ADC下重注,先后以总交易金额69亿美元、60亿美元与第一三共达成合作开发DS-8201、DS-1062,跻身史上最大BD交易之列。
ADC联合PD-1一线治疗带来的效果,也让业内看到这组合的潜力。目前,在已有多个癌种的临床试验数据显示:PD-1联用ADC展现出优异的疗效,甚至在某些癌种上具备冲击一线治疗标准的实力。
2022年12月,阿斯利康与第一三共联合宣布其抗体偶联药物(ADC)Datopotamab deruxtecan(Dato-DXd)在经大量前期治疗转移性三阴性乳腺癌(TNBC)患者身上的最新试验结果。数据显示,Datopotamab达成32%客观缓解率(ORR)。此外,在Datopotamab与PD-L1抑制剂度伐利尤单抗(Imfinzi)组合方案作为一线疗法治疗转移性TNBC患者的试验中,组合疗法达成亮眼73.6%的ORR。
2021年10 月,第一三共和阿斯利康共同宣布与默沙东达成一项临床试验合作,将启动Ⅲ期临床以评估Trop-2靶向ADC药物Dato-DXd(DS-1062)与PD-1抑制剂帕博利珠单抗联合疗法一线治疗不伴有可靶向基因突变的 PD-L1 阳性晚期/转移性 NSCLC。
据悉,该组合三期临床的开展得益于Ib期的优异数据:缓解率(ORR)为37%,叠加铂类化疗治疗ORR为41%;尤其在作为一线疗法时效果更好,疾病控制率(DCR)为100%。
另外,默沙东在三阴乳腺癌领域选择与吉利德开展合作,2021年10月,吉利德宣布与默沙东达成一项临床试验合作和供应协议,以评估吉利德Trop-2抗体偶联药物(ADC)Trodelvy(sacituzumab govitecan-hziy)联合默沙东抗PD-1 Keytruda(帕博利珠单抗)一线治疗局部晚期或转移性三阴性乳腺癌(TNBC)的疗效。
“ADC本身就是定向化疗,和PD-1/L1联和后也可能会激活免疫系统,起到1+1大于2的作用”。业内判断,ADC崛起是大势所趋,就当下来看,ADC新药有自己的PD-1或许一件好事。
本土企业争相布局
药物联用方案竞速
将市场目光拉回国内,本土创新药企的“PD-1/L1+ADC”联用同样颇具看点。
2022年,荣昌生物发布了一项维迪西妥单抗(RC-48、HER-2 ADC)联合君实生物特瑞普利单抗(PD-1单抗)用于局部晚期或转移性尿路上皮癌(UC)初步Ib/II期结果(41例受试者):ORR高达71.8%,CR为7.69%。
临床数据显示,维迪西妥单抗、特瑞普利单抗单药治疗晚期UC,ORR分别为50.5%、26%,两者的联合疗法联合疗法展现出了“1+1>2”的效果,不仅在ORR数据层面有明显改善,同时安全性有所提升(≥3级TRAE发生率为36.59%)。

除了荣昌生物的RC48与君实生物的特瑞普利单抗展开联用探索,以ADC管线为特色的Biotech公司乐普生物(美雅珂)、科伦博泰,均有PD-1管线处于商业化阶段,其中科伦博泰KL-A167注射液(PD-1)与注射用SKB264(Trop2 ADC)联用治疗非小细胞肺癌已获批临床。
从国内ADC管线布局领先的部分企业中,似乎不难看出,ADC叠加PD-1联合治疗开辟出的新赛代,有望打破单一产品的市场天花板,从而为临床差异化竞争带来机会。
作为国内PD-1商业化龙头,恒瑞医药自主研发的PD-L1抑制剂阿得贝利单抗(艾瑞利)已经成功获批,手握“PD-1”“PD-L1”两款产品,同时拥有众多临床ADC管线,涉及靶点包括HER2、cMET、Trop2等,并且已经开展了SHR-A1811(HER2 ADC)和SHR-1701(PD-L1/TGF-β融合蛋白)联用临床,恒瑞医药“PD-1/L1+ADC”探索的市场轨迹清晰可见。
“PD-1四小龙”的另外两家同样不甘示弱,百济神州引进Ambrx的定点偶联技术,同时跟踪开发免疫刺激ADC;信达生物已有两款ADC进入临床阶段,分别是IBI-343(CDN18.2 ADC)、IBI-354(HER2 ADC)。
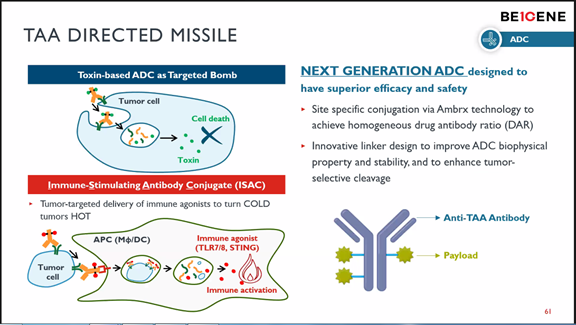
百济神州引进Ambrx的定点偶联技术,同时跟踪开发免疫刺激ADC,即抗体偶联TLR7/8激动剂
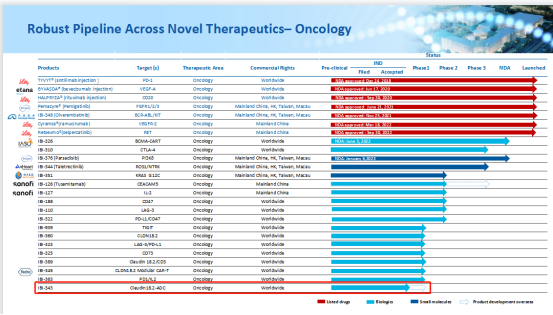
信达生物部分产品管线

信达生物在Clinicaltrials.gov网站上注册了IBI354的1/2期临床试验
目前PD-1单品销售峰值受医保谈判和竞品赠药降价的影响,远远低于之前几年的市场预期的1000亿元规模。有数据预测,年费用6万元的情况下,国内PD-1产品销售峰值约300亿;若年费用将至3万元,国内PD-1市场规模将降至235亿元。
肿瘤免疫治疗已经开启“多向”联合时代,不论与标准治疗联合向一线及新辅助治疗推进的应用,或是以“新靶点”为方向的新兴联合应用,这些基于免疫疗法的组合策略都以期提高免疫治疗的有效性、突破耐药局限或减少治疗毒副作用为目标,为肿瘤患者治疗提供更多机会。
|